|
ESTRIOL TOTAL
Método: RIA.
Muestra: suero o plasma. Separar inmediatamente y conservar a
–20°C. Orina de 24 horas.
Valor de referencia:
Suero o plasma:
Semanas de gestación
28-30= 38-140 ng/ml
30= 31-140 ng/ml
32= 35-330 ng/ml
34= 45-260 ng/ml
36= 48-350 ng/ml
38= 59-570 ng/ml
40= 95-460 ng/ml
Si se realizan determinaciones seriadas las mismas deberán ser
recolectadas en el mismo momento del día. (Se encuentran niveles
mayores al mediodía).
Orina
Hombre: 1,0-11,0 µ/día
Mujer :
Fase folicular 0-15 µg/dia
Pico ovulatorio 13-54 µg/dia
Fase lútea 8-60 µg/dia
Embarazo
Primer trimestre: 0-800 µgdia
Segundo trimestre: 800-12000 µgdia
Tercer trimestre: 5000-50000 µgdia
Significado clínico:
Es el principal estrógeno formado en la mujer embarazada. No
es secretado por el ovario de la mujer no embarazada. Posee un grupo hidroxilo
en la posición 16 y constituye más del 90% del estrógeno
conocido en la orina de la mujer embarazada, donde es secretado como glucurónido
o sulfato. El estriol es formado por un proceso biosintético único
durante el embarazo, el cual demuestra la interdependencia de feto, placenta
y madre.
Cuando la DHEA de origen fetal o materna alcanza la placenta, se forma
estrona y estradiol. Muy pequeñas cantidades son convertidas a
estriol por la placenta. Sin embargo, algo de esta DHEA sufre 16-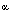 hidroxilación,
primariamente en el hígado fetal y en limitada extensión
por la adrenal fetal. Cuando la 16- hidroxilación,
primariamente en el hígado fetal y en limitada extensión
por la adrenal fetal. Cuando la 16-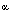 hidroxidehidroepiandrosterona sulfato
es transformada a estriol. El estriol luego es secretado
en la circulación materna. Cuando alcanza el hígado, es
conjugado a estriol sulfato, glucuronidato de estriol y a un conjugado
mixto estriol sulfoglucuronidato, en cuyas formas es excretado por la
orina materna. hidroxidehidroepiandrosterona sulfato
es transformada a estriol. El estriol luego es secretado
en la circulación materna. Cuando alcanza el hígado, es
conjugado a estriol sulfato, glucuronidato de estriol y a un conjugado
mixto estriol sulfoglucuronidato, en cuyas formas es excretado por la
orina materna.
Las concentraciones se incrementan cuando avanza la gestación
y van desde 2 mg en 24 horas en la semana 26 a 35-45 mg/24 horas a término.
El estriol también es encontrado en altas concentraciones en el
fluido amniótico y en circulación materna.
El papel del estriol en el embarazo ha sido causa de mucha especulación.
A pesar de ser un estrógeno débil, una función en
la que parece ser tan efectivo como otros estrógenos es en su capacidad
para incrementar el flujo sanguíneo útero-placentario.
Utilidad clínica:
- Monitoreo o seguimiento de embarazos de alto riesgo: medidas seriadas
reflejan la integridad del complejo fetoplacentario.
Niveles subnormales o en descenso en dos o más mediciones sucesivas
sugieren sufrimiento fetal. Una única determinación no
puede ser interpretada de manera significativa. Sin embargo, en algunos
embarazos de alto riesgo los valores de estriol pueden no encontrarse
disminuidos.
- Evaluar la edad fetal.
- Evaluar el riesgo de padecer síndrome de Down. Ver Actualizacion Estudio prenatal para síndrome de Down y defectos del tubo neural.
Variables preanalíticas:
Aumentado:
Embarazo múltiple.
Disminuido:
Prostaglandina F2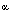 ,
postparto. ,
postparto.
Variables por enfermedad:
Disminuido:
Embarazos con alto riesgo (diabetes, preeclampsia, retardo del crecimiento
fetal, muerte fetal intrauterina, inmunización Rh, anemia, malnutrición,
pielonefritis, enfermedad intestinal, y hemoglobinopatías, hipoplasia
de las adrenales fetales, fetos anencefálicos, hiperplasia suprarrenal
congénita, deficiencia de sulfatasa placentaria).
Variables por drogas:
Aumentado:
Espirinolactona (hombres), corticoides (embarazo), barbituratos, tamoxifeno.
Disminuido:
Orina: ampicilina, neomicina, anticonceptivos orales, tiroxina, probenecid,
oxitetraciclina.
Plasma: ampicilina, albuterol, hexoprenalina, penicilina.
Interferencias (orina):
Formaldehído, galactosa, lactosa, ácido mandélico,
manosa.
Disminuido: hidroclorotiazida, laxantes, metenamina
Bibliografía:
1. Tietz N. W. Clinical Guide to Laboratory test, edited by W.B. Saunders
Company, third edition, United States of America ,1995.
2. Yen, Jaffe. Reproductive Endocrinology. Part Three. Endocrine metabolic
alterations induced by pregnanacy. Pag. 901-904. Saunders Company, third
edition, 1991.
3. Young D. Effects of Preanalytical Variables on Clinical Laboratory
Test . AACC, second edition, 1997.
4. Young D. and Friedman R. Effects of Disease on Clinical Laboratory
Test, edited by AACC, third edition, 1997.
5. Young D. Effects of Drugs on Clinical Laboratory Test, AACC, third
edition, 1990.
|